Índice de este artículo
En los procesos de osmosis, la difusión de agua a través de las membranas semipermeables es esencial para mantener un equilibrio entre las regiones intra y extra celulares de los organismos vivos. Así, las soluciones hipertónicas con su poder osmótico tienen un papel activo en el paso de este solvente.
La alta concentración de solutos en las soluciones hipertónicas tiene efectos directos sobre los cuerpos celulares, que en ocasiones se pueden observar a simple vista, tanto en organismos vegetales como animales. En este artículo explicaremos todo lo relacionado con esta solución, su concepto, sus efectos, su composición y nombraremos ejemplos para mayor compresión.
¿Qué es una solución hipertónica?
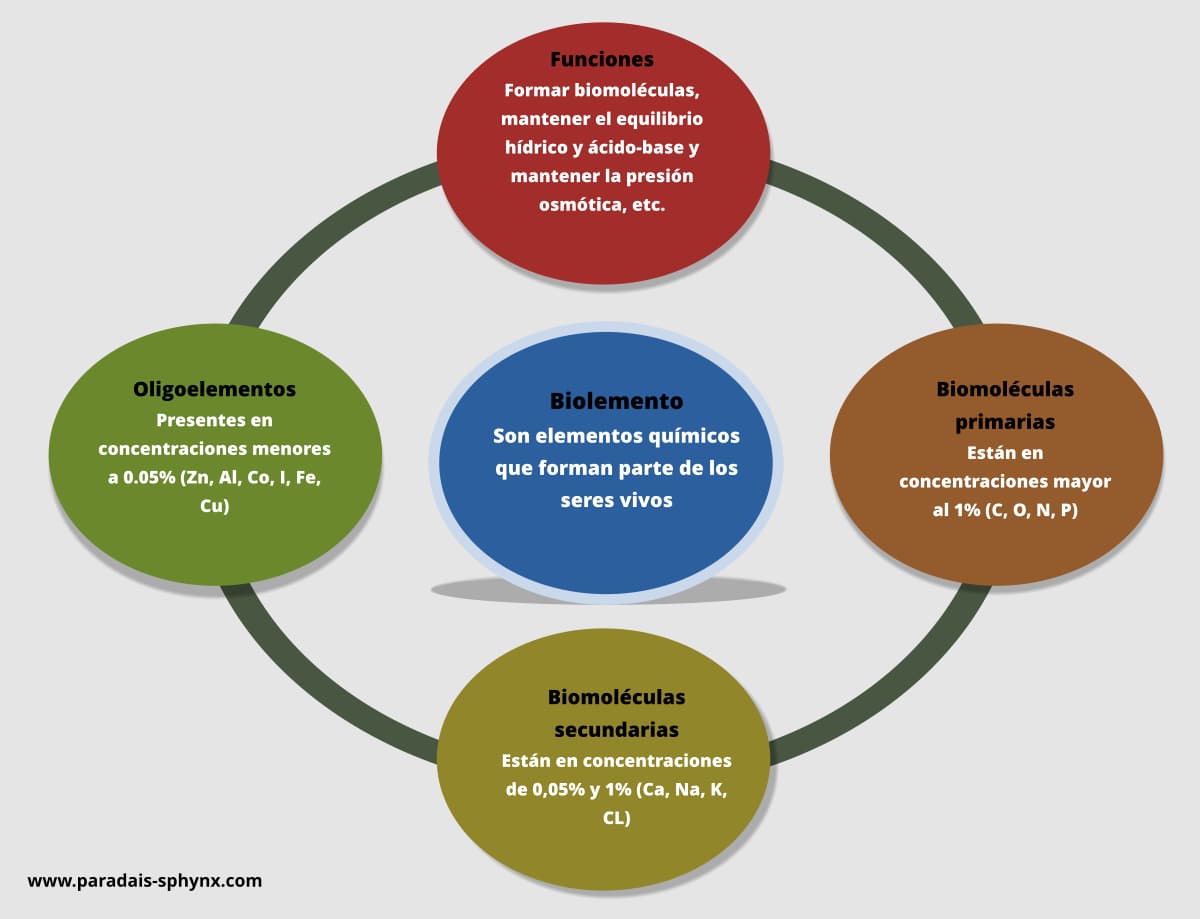
De manera sencilla, se puede definir como aquella solución que posee un alto grado de soluto en comparación con otra solución de referencia. Esta alta concentración de soluto permite que tengan un alto poder osmótico, es decir, son capaces de succionar el agua o algún solvente que se encuentra separado mediante una membrana semipermeable.
En términos biológicos se considera que una solución es hipertónica si posee mayor concentración de soluto en contraste con el plasma sanguíneo. El término hipertónico proviene del griego y se separa con el prefijo hiper cuyo significado es ¨sobre o por encima de¨ y tonos que hace referencia a la presión, por lo tanto, se dice que es una solución de alta presión.
¿Cómo funcionan?
Para comprender el funcionamiento de este tipo de solución, es necesario compararla con soluciones de referencia, siendo lo más común el plasma sanguíneo que rodea a las células de la sangre, el cual por naturaleza es isotónico. Las soluciones isotónicas mantienen un equilibrio osmótico entre los fluidos intra y extracelulares, ya que dichos fluidos se mantienen constantes en ambas regiones.
Por su parte, las soluciones hipertónicas, al poseer una mayor concentración de solutos en la solución, tienen mayor fuerza osmótica, por lo tanto, tienden a atraer o absorber los solventes de los fluidos menos concentrados. En otras palabras, el agua de las soluciones diluidas traspasa la membrana semipermeable hasta las soluciones de mayor concentración, tratando de igualar la presión osmótica en ambos lados de dicha membrana.
¿Para qué se utilizan las soluciones hipertónicas?
Este tipo de soluciones tienen un amplio uso tanto en el ámbito médico como en la industria alimentaria. Algunos de ellos son los siguientes:
Conservador de alimento: por su efecto de deshidratación en las células, incluyendo a los organismos patógenos y descomponedores como las bacterias, las soluciones hipertónicas son altamente empleados para proporcionar un medio hostil para estos microorganismos. De esta manera, se mantienen libres del crecimiento de ellas alargando la vida útil del producto, un ejemplo clásico de este tipo son las soluciones con alta carga de azúcar o frutas en almíbar.
Reposición de electrolitos: cuando hay una pérdida de electrolitos en el interior celular, se ha recomendado utilizar soluciones hipertónicas para reponerlos, estas soluciones pueden contener cierto porcentaje del electrolito que se necesite.
Aplicaciones médicas: así como para reponer electrolitos, son varias las situaciones que puede ameritar el empleo de las soluciones hipertónicas. Una de ellas es para ayudar a combatir los edemas cerebrales, reduciendo la presión intracraneal, ya que estas soluciones, por su variación de osmolaridad, arrastran el agua de la zona interior hasta los espacios intravasculares.
Otras aplicaciones médicas en la que pueden ser útiles estas soluciones son en los procesos de nebulización para controlar afecciones respiratorias como el asma. También es usada para proporcionar una vía de alimentación para aquellos pacientes que no lo pueden hacer por las vías clásicas.
Ejemplos de soluciones hipertónicas
Las soluciones con alta concentración de solutos o hipertónicas, son bastante comunes en nuestra vida diaria. Tal como se describió en la parte anterior, estos fluidos son muy utilizadas tanto en medicina como en otros ámbitos, algunos ejemplos son los siguientes:
Soluciones sobresaturadas de agua y azúcar: son soluciones empleadas para la conservación de alimentos, son conocidas bajo el nombre de almíbar. Estos jarabes son muy útiles para la conservación de frutas, donde proporcionan un medio escaso en agua, por lo tanto, los microorganismos no pueden prosperar.
Solución sobresaturada de agua y sal: al igual que la anterior, se usa para conservación de alimentos, especialmente productos cárnicos y pescado. Esta solución conocida como salmuera consiste en una combinación de agua con una proporción de sal que supera al 5 %.
Solución salina hipertónica: este tipo de fluido es empleado para diversas acciones médicas, su concentración es variable y entre las más populares están las de 3 y el 7.5 %.
Solución dextrosa: con varias aplicaciones en medicina, son soluciones con alta concentración de glucosa, por lo que también se conocen como suero glucosado. Las concentraciones varían desde el 10, 20 o 40 %.
En la naturaleza también encontramos soluciones con estas características, una de ella es el agua de mar cuya concentración de sal es superior al 3 %. Igualmente, existen zonas donde las concentraciones son mayores, siendo estas aguas incompatibles con la vida, por ejemplo, el mar muerto.
Referencias
– Astudillo, C.;Villaroel, G.; Paul, D.; Trincado, V.; Barañao, P., Méndez, M. (2016).Las nebulizaciones con solución salina hipertónica al 5% disminuyen las exacerbaciones respiratorias en pacientes pediátricos traqueostomizados. Revista Chilena de Enfermedades Respiratorias; 32: 149-154. https://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0717-73482016000300002
– Esqueda-Liquidano, M.; Gutierrez-Cabrera, J.; Cuéllar-Martínez, S.; Vargas-Tentori, N.; Ariñez-Barahona, E.; Flores-Álvarez, E.; Ruiz-Pérez, J.; Esuqeda-Liquidano, L.; Loo-Salomé, S. (2014). Edema cerebral II: tratamiento médico y quirúrgico. Medicina Interna de México; 30:687-695. https://www.medigraphic.com/cgi-bin/new/resumen.cgi?IDARTICULO=54500
– García, M.; Ardila, A. (2009). La variación del volumen celular bajo diferentes concentraciones de solución salina (NaCL). Revista Colombiana de Anestesiología; 37(2): 106-109.
– Martín, R.; Yep, G.; Sánchez, M.; Villalobos, E.; Flores, P. (2013). Estudio sobre la eficacia y utilidad de la solución salina hipertónica al 3% en la bronquiolitis aguda del lactante hospitalizado. Revista de Pediatría de Atención Primaria;15:109-15.